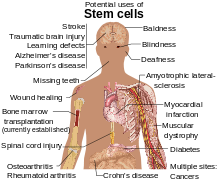
العلاج باستخدام الخلايا الجذعية هو زراعة خلايا بشرية أو حيوانية لتعويض الخلايا أو الأنسجة التالفة في محاولة لعلاج الأمراض. قد يستخدم العلاج الخلوي والعلاج الجيني معا للوصول لأفضل النتائج. أي استخدام الخلايا الجذعية للعلاج او الوقاية من مرض او حالة معينة. و زراعة النخاع العظمي هو العلاج بالخلايا الجذعية الأكثر استخداما لكن بعض العلاجات المشتقة من دماء الحبل السري تستخدم أيضا. و لا يزال البحث جار في طريقه لتطوير مصادر مختلفة للخلايا الجذعية و لاستخدام هذه الخلايا في معالجة أمراض الأعصاب التنكسية ، السكري، أمراض القلب و حالات اخرى. مع قدرة العلماء على عزل و زراعة خلايا الجنين الجذعية، و مع تزايد مقدرتهم في إنتاج الخلايا الجذعية عن طريق نقل نواة الخلية الجسدية و تقنيات لخلق الخلايا الجذعية المحفزة متعددة القدرات ظهر الجدل بما يتعلق بسياسة الإجهاض و الاستنساخ البشري. كما أثارت الجهود التي تسوّق العلاج المرتكز على زراعة دماء الحبل السري المخزنة الجدل و الخلاف.
محتويات
1 الاستخدامات الطبية
2 البحث
2.1 التنكس العصبي
2.2 إصابات الدماغ والحبل الشوكي
2.3 القلب
2.4 تكوين خلايا الدم
2.5 الأسنان المفقودة
2.6 إعادة نمو خلايا شعر القوقعة
2.7 العمى وضعف الرؤية
2.8 السكري
2.9 جراحة تقويم العظام
2.10 شفاء الجروح
2.11 العقم
2.12 الايدز ( متلازمة نقص المناعة )
2.13 التجارب السريرية
3 حيوانات أخرى
3.1 تطبيقات بيطري
3.2 تطوير نماذج العلاج التجديدية
3.3 مصادر الخلايا الجذعية
3.4 الخلايا الجذعية وإصلاح النسيج الصلب
3.5 الخلايا الجذعية وإصلاح العظام
3.5.1 إصلاح الأوتار
3.5.2 تصليح المفصل
3.5.3 إصلاح خلل العظام
3.6 الخلايا الجذعية وإصلاح العضلات
3.7 الخلايا الجذعية وإصلاح الجهاز العصبي
3.7.1 التهاب القرنية والملتحمة الجاف (KCS)
3.8 المناطق الحالية للبحث
3.8.1 الخلايا الجذعية في المختبر
3.8.2 الخلايا الجذعية وحفظها
3.8.3 الاستخدامات السريرية في المستقبل
4 الجدال حول الخلايا الجذعية الجنينية
5 حول العالم
5.1 الصين
5.2 الشرق الأوسط
5.3 المكسيك
5.4 كوريا الجنوبية
5.5 تايلند
5.6 أوكرانيا
5.7 الدول الأخرى
الاستخدامات الطبية
معلومات اضافية: زرع الخلايا الجذعية المتعلقة
بتكون الدم.
على مدى ثلاثين سنة، تم استخدام النخاع العظمي لعلاج مرضى
السرطان المصابين بأمراض مثل
ابيضاض الدم والورم اللمفي؛ هذا هو الشكل الوحيد من أشكال العلاج بالخلايا الجذعية الذي يمارس على نطاق واسع. أثناء المعالجة الكيميائية، تموت معظم الخلايا المتنامية بالعوامل السامة للخلايا. مع ذلك لا تستطيع هذه المواد التمييز بين ابيضاض الدم أو الخلايا الورمية والخلايا الجذعية المتعلقة بتكون الدم الموجودة في النخاع العظمي. هذا هو الأثر الجانبي من استراتيجيات
العلاج الكيميائي التقليدي الذي يحاول زرع الخلايا الجذعية عكسه؛ النخاع العظمي الصحي للمتبرع يعيد الخلايا الجذعية الفعالة لاستبدال الخلايا المفقودة والتالفة في جسم المضيف خلال فترة العلاج. الخلايا المزروعة تولد ايضًا
استجابة مناعية تساعد على قتل
الخلايا السرطانية؛ لكن هذة العملية قد تخرج عن السيطرة و تؤدي إلى داء الطعم حيال الثوي والذي يعد أخطر الآثار الجانبية لهذا العلاج.
هنالك نوع آخر من العلاج باستخدام الخلايا الجذعية و يسمى
بروشيمال، تمت الموافقة عليه بشروط في كندا عام 2012 للسيطرة على داء الطعم حيال الثوي الحاد في الأطفال الذين لم يستجيبوا للمنشطات إنه علاج جذعي خيفي يعتمد على علاج اللحمة المتوسطة الجذعية (MSCs) المشتقة من النخاع العظمي لدى المتبرع البالغ. يتم تنقية الMSCs من النخاع، زراعتهم وتعبئتهم، مع ما يصل إلى 10،000 جرعات مستمدة من متبرع واحد. تخزن الجرعات مجمدة لحين الحاجة إليها.
وافقت إدارة الأغذية والعقاقير على خمسة منتجات للخلايا الجذعية المتعلقة بتكون الدم المستمدة من دماء الحبل السري، لعلاج
أمراض الدم والمناعة.
في مارس 2016 علاج Strimvelis شركة جلاكسو سميث كلاين (GSK 2696273) لعلاج
-SCID ADA وأوصى للحصول على موافقة الاتحاد الأوروبي.
البحث
التنكس العصبي
الأمراض والحالات التي يكون فيها العلاج بالخلايا الجذعية واعد أو قيد الإنشاء.
إن أدمغة البالغين الأصحاء تحتوي على خلايا جذعية عصبية تقسم إما للحفاظ على أعداد الخلايا الجذعية عامة، أو لتصبح خلايا السلف. في الحيوانات البالغة، تهاجر خلايا السلف داخل الدماغ وتعمل في المقام الأول للحفاظ على
الخلايا العصبية للشم. تم الإبلاغ أن التفعيل الدوائي للخلايا الجذعية العصبية داخلية المنشأ يحث على الحماية العصبية و الشفاء السلوكي في نماذج الفئران البالغة التي تعاني من
اضطراب عصبي.
إصابات الدماغ والحبل الشوكي
السكتة الدماغية وإصابات الدماغ الرضحية تؤدي إلى موت خلوي، يتميز بفقدان الخلايا العصبية و oligodendrocytes داخل الدماغ. كانت
تجربة سريرية صغيرة تجري في اسكتلندا في عام 2013، حيث تم حقن الخلايا الجذعية في أدمغة مرضى السكتة الدماغية.
أجريت دراسات سريرية وحيوانية لاستخدام الخلايا الجذعية في حالات إصابات
الحبل الشوكي.
القلب
تم مؤخرا الكشف عن الكثير من التناقضات في الأعمال الأولية التي سجلت ل Bodo-Eckehard Strauer فمن خلال تجارب سريرية عديدة في بعض المختبرات تم إثبات العلاج بالخلايا الجذعية البالغة كوسيلة فعالة، ناجحة وآمنة في حالات الاحتشاءات القديمة والحديثة والفشل القلبي الغير ناتجة عن احتشاء العضلة القلبية. بينما أثبتت الدراسات الأولية على الحيوانات نتائج علاجية رائعة ، كانت التجارب السريرية ذات نتائج مقبولة إحصائيا . ومن الأسباب المحتملة لهذا الاختلاف والفرق في النتائج أعمار المرضى، توقيت العلاج وجود احتشاء بالعضلة القلبية مؤخرا ومن الممكن التغلب على هذه العوائق من خلال علاج إضافي يزيد فاعلية العلاج بالخلايا الجذعية أو يجعل الطريقة أكثر فاعلية. أما عن الدراسات الحديثة فهي تختلف كثيرا بتقنيات المعالجة و أنواع الخلايا وتوقيت وطريقة العلاج و الخصائص التي تمت دراستها مما يجعلها صعبة المقارنة وهنا تظهر الحاجة لأبحاث المقارنة .
ومن الخلايا الجذعية المستخدمة في علاج احتشاء عضلة القلب الخلايا الجذعية المشتقة من نخاع العظم الذاتي ومن الممكن استخدام خلايا جذعية ناضجة مشتقة من النسيج الشحمي (الدهني) وقد كان استخدام الخلايا الجذعية الناضجة في علاج أمراض القلب متوافر تجاريا في خمس قارات على الأقل في عام 2007 [citation needed]
من الطرق المستخدمة بالعلاج:
توليد خلايا عضلية قلبية
تحفيز نمو أوعية دموية جديدة لإعادة تأهيل الأنسجة المتضررة
إفراز عوامل النمو
استخدام طرق علاجية أخرى
ومن المحتمل تمايز خلايا نخاع العظم الناضجة إلى خلايا عضلية قلبية
حدثت أول عملية دمج ناجحة من الخلايا القلبية المشتقة من خلايا جنينية بشرية في خنازير غينية في أغسطس عام 2012، وقد تم تسجيل قوة انقباض القلب بعد أربعة أسابيع من تعريض الخنازير لجلطة قلبية وعلاجها وقد انقبضت الخلايا بقوة متزايدة ولكن لم يعرف ما إذا كانت النتائج الإيجابية قد حصلت بفعل التأثير الكهربائي الحركي الناتج من الخلايا البشرية. وستركز الأبحاث المستقبلية على زراعة الخلايا حول الأنسجة المتضررة بشكل قوي ومعرفة أي المصدرين (الخلايا الجذعية الجنينية أو الناضجة) هو الأكثر فاعلية في العلاج
وقد احتوت تقاريرعام 2013 - والتي تناولت التأثيرات القوية و المفيدة للخلايا الجذعية الذاتية المشتقة من نخاع العظم على وظيفة البطين في القلب - على الكثير من الاختلافات وبشكل عام، فإن عدد المرضى الذين أعلن عن تجريب العلاج بالخلايا الجذعية عليهم أكثر من عدد الخلايا الجذعية المعالجة في المختبرات، وقد تم إجراء تحقيق عالمي في هذا الموضوع أغلق في عام 2012 بدون أي نتائج وقد أعيد فتحه عام 2013
وتعتبر فائدة استخدام المعالجة بالخلايا الجذعية للنسيج القلبي وتجديده بعد أي حالة فشل قلبي أو تضرر بالأنسجة من المجالات الطبية الواعدة
في البداية كانت التطورات في مجال المعالجة مرتبطة بشكل نسبي على قدرة خلايا نخاع العظم على التمايز إلى خلايا قلبية؛ بحيث كانت قدرة الخلايا غير المعدلة على التمايز إلى نسيج قلبي غير كافية، ولكنّ تطور تقنيات حديثة واعدة في مجال معالجة وتعديل الخلايا لتتمايز إلى خلايا قلبية مولدة قبل زراعتها سهّل هذه العملية
تكوين خلايا الدم
ما يميز
الخلايا المناعية المرجعية البشرية أنها تسمح للجسم البشري في الدفاع عن نفسه من المستضدات سريعة التكيف. و مع ذلك فإن
الجهاز المناعي هو عرضة للتفكك مع تكون المرض وبسبب الدور الحاسم الذي يلعبه في الدفاع العام، فإن تدهوره غالبًا ما يكون قاتل للكائن الحي ككل ويتم تشخيص أمراض الخلايا المكونة للدم وتصنيفها عبر التخصصات الفرعية لعلم الأمراض المعروفة باسم أمراض الدم خاصية الخلايا المناعية هي التي تسمح للجسم بالتعرف على المستضدات الغريبة مما يتسبب في مزيد من الصعوبة في علاج أمراض المناعة. يجب أن يتطابق النسيج المتبرع به مع أنسجة المتبرع له لنجاح عملية زراعة النسيج، ولكن الحصول على أنسجة متوافقة غير شائع، حتى بين الأقارب من الدرجة الأولى. إن البحوث باستخدام كل من الخلايا الجذعية المكونة للدم عند الكبار
والخلايا الجذعية الجنينية فتحت المجال لدراسة آليات وطرق العلاج الممكنة لكثير من هذه الامراض.
يمكن توليد
خلايا دم حمراء بشرية ناضجة تمامًا بواسطة خلايا جذعية مكونة للدم، والتي هي خلايا بدائية لتكوين الدم خارج الجسم البشري. في هذه العملية، تزرع الخلايا الجذعية المكونة للدم جنبًا إلى جنب مع الخلايا اللحمية، مما يخلق بيئة تحاكي ظروف نخاع
العظام، وهو الموقع الطبيعي لنمو خلايا الدم الحمراء الإريثروبويتين، وهو عامل نمو، يضاف لجعل الخلايا الجذعية تستكمل التمايز النهائي لتكوين خلايا الدم الحمراء تطوير
البحث العلمي في هذه التقنية من الممكن أن يحقق فوائد محتملة في مجالات العلاج بالجينات
ونقل الدم والعلاج بالأدوية الموضعية.
الأسنان المفقودة
في عام 2004، اكتشف العلماء في كلية كنجز في لندن طريقة لزراعة(cultivate) سن كامل في الفئران وكانوا قادرين على تنمية
الأسنان المهندسة بيولوجيًا القائمة بذاتها في المختبر. إن الباحثين واثقون من أن تكنولوجيا تجدد الأسنان يمكن أن تستخدم لزراعة الأسنان الحية في المرضى البشر. من الناحية النظرية، الخلايا الجذعية المأخوذة من المريض يمكن أن (coaxed) في المختبر إلى أن تتحول إلى برعم السن، والتي عند زراعتها في
اللثة سوف تعطي أسنانًا جديدة، ويتوقع أن تكون نمت في وقت أكثر من ثلاثة اسابيع وسوف تلتحم مع عظم
الفك وتفرز مواد كيميائية تشجع
الأعصاب والأوعية الدموية على الاتصال معها. وهذه العملية شبيهة لما يحدث عندما ينمو البشر أسنانهم الأصلية. لا يزال هنالك العديد من التحديات، مع ذلك، قبل أن تصبح الخلايا الجذعية خيارًا لاستبدال الأسنان المفقودة في المستقبل.
لا يزال البحث مستمرًا في مختلف المجالات، في التماسيح التي هي(polyphyodonts) تنمو الأسنان اللاحقة لتصل إلى 50 مرة(أسنان بديلة صغيرة) تحت كل سن عملي ناضج للاستبدال مرة في السنة
إعادة نمو خلايا شعر القوقعة
أفادت الباحثة هيلير نجاحها في إعادة إنماء الخلايا الشعرية للقوقعة باستخدام خلايا جذعية جنينة
العمى وضعف الرؤية
منذ عام 2003، نجح الباحثون بزراعة خلايا
القرنية الجذعية في العيون المتضررة لاستعادة النظر. "تحصد من
الأجنة المجهضة صفائح من خلايا
الشبكية المستخدمة من قبل الفريق، والتي يجدها بعض الناس مرفوضة." عندما تزرع هذه الصفائح على القرنية المتضررة، تحفز الخلايا الجذعية تجديد الإصلاح، واستعادة الرؤية في نهاية المطاف. وكانت أحدث هذه التنمية في يونيو 2005، عندما استطاع باحثون في مستشفى الملكة فيكتوريا في ساسكس إنجلترا استعادة نظر أربعين مريض باستخدام نفس التقنية. تمكنت المجموعة بقيادة شيراز دايا من استخدام الخلايا الجذعية التي تم الحصول عليها من المريض، قريب أو حتى جثة بنجاح. ما تزال التجارب جارية.
في أبريل 2005، زرع أطباء في المملكة المتحدة خلايا قرنية جذعية من متبرع بالأعضاء إلى قرنية ديبورا كايتلن، وهي امرأة أصيبت
بالعمى في إحدى عينيها عندما ألقي حامض في عينها في ملهى ليلي. القرنية، التي هي الغطاء الشفاف للعين، تعد موقعًا مناسبا جدًا للزراعة. في الواقع، كانت أول عملية زراعة أعضاء ناجحة في الإنسان هي عملية
زرع القرنية. إن غياب الأوعية الدموية داخل القرنية يجعل من هذه المنطقة هدفًا سهلًا نسبيًا للزراعة. إن أغلبية عمليات زراعة القرنية التي تجرى حاليًا هي من أجل مرض تحللي في القرنية يعرف
بالقرنية المخروطية.
أفادت تقارير مستشفى جامعة نيو جيرسي أن نسبة النجاح لنمو خلايا جديدة من الخلايا الجذعية المزروعة يتراوح من 25 في المئة إلى 70 في المئة.
في عام 2014، أظهر الباحثون أن الخلايا الجذعية التي تم جمعها كخزعات من القرنيات البشرية المتبرع بها قد تمنع تكون الندوب دون إثارة الرفض في فئران ذوي القرنيات المتضررة
في يناير 2012، نشرت مجلة لانسيت ورقة علمية لستيفن شوارتز، في معهد جولز ستاين لأمراض العين التابع لجامعة كاليفورنيا لوس أنجلوس، تذكر حالة امرأتين أصيبتا قانونيًا بالعمى نتيجة لمرض ضمور بقعة الشبكية ،وأنهما شهدتا تحسنًا جذريًا في مستوى الرؤية بعد حقن الشبكية بخلايا جذعية جنينة بشرية.
في يونيو 2015، نشرت دراسات طب العيون بالخلايا الجذعية (اسكتلندا) الذي يعتبر أكبر دراسات الخلايا الجذعية البالغة في طب العيون (www.clinicaltrials.gov NCT # 01920867) النتائج الأولية على المريض مع مرض العصب البصري الذي تحسن من 20/2000 إلى 20 / 40 بعد العلاج بنخاع الخلايا الجذعية المشتقة من العظام
السكري
يفقد مرضى السكري وظيفة
خلايا بيتا المنتجة
للأنسولين في
البنكرياس في التجارب الحديثة، كان العلماء قادرون على تحويل الخلايا الجذعية الجنينية إلى خلايا بيتا في المختبر. من الناحية النظرية إذا تمت زراعة خلايا بيتا بنجاح، سيتمكن العلماء من استبدال الخلايا العاطلة عن العمل في مرضى السكري
نقل وزراعة الأعضاء
يمكن تنمية الخلايا الجذعية الجنينية البشرية في
مزرعة خلوية وتحفيزها لتكوين خلايا منتجة للإنسولين، التي من الممكن زرعها في جسم المريض.
مع ذلك، فإن النجاح السريري يعتمد بشكل كبير على تطوير العمليات التالية:
الخلايا المزروعة يجب أن تتكاثر
الخلايا المزروعة يجب أن تفرق بطريقة خاصة بالموقع
الخلايا المزروعة يجب أن تبقى على قيد الحياة في جسم المتلقي (تفادي رفض الزراعة)
الخلايا المزروعة يجب أن تتداخل مع
الأنسجة المستهدفة
الخلايا المزروعة يجب أن تقوم بإعادة وظيفة الخلايا المستقبلة عن طريق التداخل مع البيئة المضيفة
جراحة تقويم العظام
تم الإبلاغ عن دراسات سريرية في علاج حالات جراحة تقويم العظام. إلى الآن، يبدو أن التركيز في دراسة رعاية
العضلات يتمحور حول الخلايا الجذعية المتعلقة باللحمة المتوسطة. نشر سينتينو دليلًا على زيادة حجم
الغضروف والهلالة في الأفراد الخاضعين (كلا على حدة) عن طريق صورة
رنين مغناطيسي. لم تنشر نتائج التجارب التي تشمل عددًا كبيرًا من الأفراد الخاضعين بعد. مع ذلك، صدرت دراسة سلامة أجريت على 227 مريض على مدى 3-4 سنوات تظهر سلامة كافية وحد أدنى من المضاعفات المرتبطة بالخلايا الجذعية المتعلقة باللحمة المتوسطة
ونشر واكيتاني أيضًا سلسلة قضايا صغيرة تتكون من تسعة عيوب في خمس ركب تحوي زراعة جراحية للخلايا الجذعية المتعلقة باللحمة المتوسطة مع تغطية العيوب الغضروفية المعالجة.
شفاء الجروح
من الممكن أيضًا استخدام الخلايا الجذعية لتحفيز نمو الأنسجة البشرية. في البالغين، عادة ما تستبدل الأنسجة المتضررة بالندب، التي تتميز
بالجلد ببنية
كولاجين غير منتظمة، فقدان بصيلات الشعر وبنية غير منتظمة في الأوعية الدموية. في حال تضرر الأنسجة الجنينية، على أي حال، يستبدل النسيج المتضرر بنسيج طبيعي عن طريق الخلايا الجذعية هنالك طريقة ممكنة لتجديد النسيج عند البالغين وهي وضع خلية جذعية بالغة "بذور" داخل سرير أنسجة "تربة" في سرير الجرح والسماح للخلايا الجذعية بتحفيز التمايز في خلايا سرير النسيج. هذه الطريقة تظهر استجابة للتجديد أقرب ما تكون لشفاء الجروح الجنينية من تشكل الندوب لدى البالغين. لا يزال الباحثون يتحرون جوانب مختلفة من "تربة" الأنسجة المؤدية إلى التجديد
العقم
تم تحفيز الخلايا الجذعية الجنينية البشرية لتنتج خلايا شبيهة بخلايا النطفة، ومع ذلك لا يزال هنالك تشوه بسيط. ومن الممكن أن يعالج
فقد النطاف بكفاءة عالية.
في عام 2012، تم عزل خلايا بزرة البيضة الجذعية من مبايض الإنسان والفئران البالغة وبرهنت أنها قادرة على إنتاج بويضات ناضجة. وهذه الخلايا لديها القدرة على علاج
العقم.
الايدز ( متلازمة نقص المناعة )
تدمير جهاز المناعة من قبل فايروس نقص المناعة المكتسبة(الإيدز) مُقاد من قبل خساره CD4+ وهو بروتين سكري يكون على سطح خلايا T المناعية المساعدة في الدم والعقد الليمفاوية، الدخول الفايروسي لخلايا CD4+ يتم بواسطة التفاعل مع مستقبِلات التنشيط الكيميائي على سطح الخلايا، بالمجمل هما CcR5 و CXR41 أي أنهما هما المواقع التي يرتبط عليها الفيروس؛ وذلك لأن عملية تتابع التناسخ وتكاثر الفيروس تحتاج لجين خلوي لعملية التكثير، خلايا CD4+ تكون الهدف الأوّلي لفايروس نقص المناعة المكتسبة. مؤخرا قام العلماء بعمليات استقصاء وتحقيق في عمليات بديلة لعلاج للفيروس، بناء على تصنيع جهاز مناعة مُقاوم للمرض من خلال زرع خلايا ذاتية المنشأ، جينات معدّلة (مقاومة للمرض)، والخلايا الجذعية المكوُّنة لخلايا الدم الحمراء، والخلايا المولدة(GM-HSPC) .
التجارب السريرية
GRNOPC1 في 23 من كانون الثاني لعام 2009، أعطت منظمة الغذاء والدواء الأمريكية التخليص لشركة جيرون لبدء أول تجربة سريرية على الخلايا الجذعية الجنينية على البشر. هذه التجربة تهدف إلى تقييم الدواء GRNOPC1 ( وهو خلايا جذعية مشتقة من خلايا مولدة قليلة التفرع )، على المرضى الذين يعانون من إصابات خاصة في النخاع الشوكي. التجربة تم إيقافها في نوفمبر 2011 حتى يتسنى للشركة أن تركز على العلاجات في"البيئة الحالية لندرة رأس المال والظروف الاقتصادية غير المحتمة". في عام 2013 اكتسبت التكنولوجيا الحيوية وشركة الطب المتجدد صفقة جيرون للخلايا الجذعية، بهدف استئناف التجارب السريرية
استخدام الخلايا الجذعية المخزنة مسبقا لقد رأى الخبراء العلميون أن استخدام الخلايا الجذعية بعد تخزينها وتجميدها لفترة يقلل من فاعليتها في العلاج وقدرتها على التمايزمقارنة بالخلايا الجذعية الحديثة ( الطازجة ) والتي تعد في طور النمو؛ لذلك يجب إعادة زراعة وتنمية الخلايا الجذعية المخزنة مسبقا لتصبح في طور النمو قبل استخدامها في العلاج السريري، حيث أثبتت الكثير من التجارب السريرية التي استخدمت الخلايا المخزنة مباشرة دون إعادة زراعتها فشلها مقارنة بتلك التجارب التي أعادت نموها وتربيتها
حيوانات أخرى
تطبيقات بيطري
توزيعات الجهد على الطب البيطري
الأبحاث حاليًا تطبق على الخيول، الكلاب والقطط، التي من الممكن أن تكون مفيدة في تطوير العلاج بالخلايا الجذعية في
الطب البيطري وتستهدف نطاق واسع من الإصابات والأمراض مثل
احتشاء عضلة القلب، السكتة الدماغية وتأذي
الأوتار والأربطة،
التهاب المفاصل، والداء العظمي الغضروفي والضمور العضلي كلاهما في الحيوانات الكبيرة، كما الإنسان. بينما الأبحاث التي تعتمد على العلاجات المرتكزة على
الخلية بشكل عام تعكس الاحتياجات الطبية الإنسانية،الدرجة العالية من التواتر وحدة بعض الإصابات في سباق الخيول وضعت الطب البيطري في طليعة هذا النهج الروائي التجديدي. مزاملة الحيوانات تستطيع أن تخدم بطريقة طبية سريرية عدة نماذج ذات صلة مع الأمراض البشرية تطوير نماذج العلاج التجديديةيعتقد أن الخلايا الجذعية تساعد على الترميم عن طريق خمسة آليات أساسية: 1) منح أثر مضاد للالتهابات. 2) تستهدف الأنسجة المتضررة وتجنيد خلايا أخرى مثل خلايا السلف البطانية، الضرورية لنمو الأنسجة. 3) دعم إعادة تشكيل النسيج المساندة على تشكيل الندبة. 4) تثبيط موت الخلايا المبرمج. 5) تستطيع الانقسام إلى أنسجة عظمية،غضروفية،وترية ورابطة.
من أجل توفير التغذية الدموية للمناطق المتضررة، وبالتالي تحفز تجديد الأنسجة،
الصفائح الدموية الغنية
بالبلازما من الممكن أن تستخدم مع زراعة الخلايا الجذعية. فعالية بعض الخلايا الجذعية من الممكن أن تتأثر في أسلوب التوصيل؛ على سبيل المثال، لتجديد
العظم، الخلايا الجذعية عادة ما تقدم على سقالة بحيث تنتج المعادن الضرورية لتكوين العظم الوظيفي.
تبين أن الخلايا الجذعية تمتلك مناعة منخفضة بسبب العدد القليل نسبيًا من جزيئات التوافق النسيجي الرئيسي المركبة المتواجدة على سطحها.إضافة إلى ذلك وجد أنها تفرز منشطات كيميائية تقوم بتغيير
الاستجابة المناعية وتزيد القدرة الاحتمالية للنسيج الجديد. هذا يسمح للعلاج الخيفي بأن يطبق من دون خطورة رفض مرتفعة
مصادر الخلايا الجذعية
التطبيقات البيطرية لعلاج الخلايا الجذعية كوسيلة من وسائل تجديد الأنسجة شكلت بطريقة كبيرة عن طريق البحث الذي بدأ مع استخدام الخلايا الجذعية اللحمية البالغة من أجل علاج الحيوانات التي تعاني من إصابات أو عيوب مؤثرة على
العظم، الغضروف،
الأربطة و\أو الأوتار هناك فئتان من الخلايا الجذعية تستخدم في العلاجات: خلايا جذعية خيفية مشتقة من واهب جيني مختلف من نفس الأصناف وخلايا جذعية لحمية ذاتية المنشأ، المشتقة من مريض قبل استخدامها في علاجات مختلفة فئة ثالثة، خلايا جذعية ذو جينات خارجية، أو خلايا جذعية مشتقة من اصناف مختلفة، تستخدم بشكل أولي لأهداف دراسية خاصة للعلاجات البشرية
معظم الخلايا الجذعية معدة للعلاج التجديدي التي هي منعزلة بشكل عام إما من نخاع العظم للمريض أو من
النسيج الدهني. الخلايا الجذعية اللحمية من الممكن أن تتمايز لخلايا بناءة للعظم، غضروف، أوتار وأربطة كما
العضلة، عصبي وأنسجة سلف أخرى، لطالما درس الصنف الرئيسي من الخلايا الجذعية في علاج الأمراض التي تؤثر على هذه الأنسجة. عدد الخلايا الجذعية التي تم نقلها وزراعتها للنسيج المتضررة من الممكن أن تغير فعالية العلاج. وفقًا لذلك، الخلايا الجذعية المأخوذة من شفاطات نخاع العظم، على سبيل المثال، تزرع في مختبرات متخصصة من أجل أن نموها لملايين الخلايا. رغم أن النسيج المشتق من
الدهون يتطلب عملية سابقة للاستخدام، منهجية الزراعة للخلايا الجذعية المشتقة من الدهن غير واسعة النطاق كما الخلايا المشتقة من نخاع العظم في حين إنه يعتقد أن الخلايا الجذعية المشتقة من نخاع العظم مفضلة لإصلاح العظم، الغضروف، الأربطة والوتر، يعتقد آخرون أن تقنيات التجميع ذات الصعوبة الأقل والبيئة المتعددة الخلايا المكروية متواجدة في كل الأحوال في أجزاء الخلايا الجذعية المشتقة من الدهن مما يجعل الأخير مصر مفضل لنقل وزراعة الخلايا ذاتية المنشأ.
مصادر جديدة من الخلايا الجذعية اللحمية، حاليًا موضع للبحث، متضمنة الخلايا الجذعية الموجودة في الجلد وطبقة الجلد الداخلية التي هي محط اهتمام بسبب التخفيف الذي من الممكن أن يتم حصاده مع أقل خطورة للحيوان الخلايا الجذعية الدموية تم اكتشاف أنها تنتقل في
الدورة الدموية وتملك قدرة تمايز كافية كما الخلايا الجذعية اللحمية الأخرى، مرة أخرى مع تقنية حصاد غير اجتياحية
حاليًا هناك المزيد من الاهتمام في استخدام خلايا جذعية لحمية لا جنينية. حاليًا الأبحاث في طريقها لتجربة قدرات الخلايا الجذعية للتمايز الموجودة في الحبل السري،
الكيس المحي والمشيمة للحيوانات المختلفة. يعتقد أن الخلايا الجذعية لديها قدرة تمايز أكثر من نظرائها الناضجة، يتضمن قابلية الأنسجة التي شكلت بالفعل ذات مصدر
أديم باطن لو أذيم باطن.
الخلايا الجذعية وإصلاح النسيج الصلب
بسبب القابلية الإيجابية العامة للشفاء للخلايا الجذعية، اكتسبت الاهتمام لعلاج الجروح الجلدية. هذا الاهتمام العالي لهؤلاء ذو المقدرة الشفائية المنخفضة، مثل مرضى السكري، وهؤلاء الذين يخضعون للعلاج الكيميائي. في تجربة واحدة، الخلايا الجذعية عزلت من هلام وارتون الخاص بالحبل السري. هذه الخلايا حقنت بشكل مباشر في الجروح. في ظرف أسبوع، تمت إعادة بناء خلايا باطنية بشكل كامل للجروح، مقارنة بإعادة بناء الخلايا الباطنية الثانوية في عملية التعامل مع الجروح. هذا أيضًا يظهر القابلية للخلايا الجذعية اللحمية في إصلاح النسيج الخارجي للجلد
عيوب
الحنك الرخو في الخيول بسبب الفشل الجنيني للغلق التام في خط الوسط خلال مرحلة التكوين الجنيني. هذا عادة لا نجده لغاية إلا عندما يصبح أسوأ بسبب صعوبة رؤية الحنك الرخو بشكل كامل. يعتقد أن قلة نسبة النجاح في المداخلات الجراحية لإصلاح العيوب يوعز إلى قلة القدرة على رؤية الحنك الرخو. بالمحصلة، عادة ما تنتهي هذه الحالة بالموت الرحيم للحصان. حاليًا، استخدام الخلايا الجذعية اللحمية للعلاجات التقليدية. بعدما يقفل الجراح الحنك، تحقن خلايا لحمية ذاتية المنشأ في الحنك الرخو. وجد أن الخلايا الجذعية تتداخل في عملية شفاء النسيج خاصة على طول حد النسيج القديم. كما يوجد انخفاض كبير في عدد الخلايا الالتهابية، التي يعتقد أنها تساعد في عملية الشفاء.
الخلايا الجذعية وإصلاح العظام
وكانت العلاجات المستندة إلى الخلايا الجذعية ذاتية المنشأ لإصابات الأربطة، والأوتار، التهاب المفاصل، داء العظم الغضروفي، وخراجات العظام شبه الغضروفي متاحة تجاريًا لمزاولة الأطباء البيطريين لعلاج الخيول منذ عام 2003 في الولايات المتحدة، ومنذ عام 2006 في المملكة المتحدة. وأصبحت متاحة العلاجات القائمة على الخلايا الجذعية ذاتية المنشأ لإصابات الأربطة، والأوتار، التهاب المفاصل، في الكلاب للأطباء البيطريين في الولايات المتحدة منذ عام 2005. وأكثر من 3000 خيول وكلاب مملوكة لدى قطاع الخاص تم علاجها باستخدام الخلايا الجذعية الدهنية المشتقة ذاتية المنشأ. وقد ظهرت فعالية هذه العلاجات في
تجارب سريرية مزدوجة التعمية للكلاب التي تعاني من التهاب المفاصل في الورك
والكوع والخيول التي تعاني من ضرر في الأوتار
إصلاح الأوتار
الخيول التي تستخدم في السباق عرضة وبشكل خاص لإصابات الأوتار والأربطة. إن العلاجات التقليدية غير ناجحة في إعادة قدرة الحصان على العمل بشكل كامل.
العلاج الطبيعي، مسترشد في ذلك العلاجات التقليدية، يؤدي إلى تكون
ندبة ليفية والتي بدورها تقلل من مرونة وحركة المفاصل الكاملة. منعت العلاجات التقليدية عددًا كبيرًا من الخيول من العودة إلى النشاط الكامل، ولدى هذه العلاجات أيضًا نسبة عالية من إعادة الإصابة نظرًا لطبيعة الوتر الصلبة. إن إدخال كل من نخاع العظم والخلايا الجذعية الدهنية المشتقة، بجانب التحفيز الميكانيكي الطبيعي عزز تجديد أنسجة الوتر. روجت الحركة الطبيعية محاذاة الألياف الجديدة والتيندوسايتس مع المحاذاة الطبيعية الموجودة في الأوتار السليمة. إن العلاج بالخلايا الجذعية لم يسمح لمزيد من الخيول بالعودة إلى العمل بشكل الكامل فقط بل أيضًا قلص إلى حد كبير معدل إعادة الإصابة على مدى فترة ثلاث سنوات أو أكثر
وفي الآونة الأخيرة، تم تطبيق استخدام الخلايا الجذعية الجنينية لإصلاح الأوتار. وقد أظهرت الخلايا الجذعية الجنينية أن لديها معدل أفضل من خلايا البالغين الجذعية للبقاء على قيد الحياة في الأوتار وأن لديها أيضًا مقدرة أفضل على الهجرة للوصول إلى جميع المناطق التالفة في الوتر. وكانت أيضًا نوعية الإصلاح الشامل لدى هذه الخلايا أعلى، مع بنية وتر وتشكيل كولاجين أفضل. ولم يظهر هنالك أي ورم خلال الفترة التجريبية( ثلاثة أشهر). يجب إجراء دراسات طويلة الأجل التي يتعين الاضطلاع عليها لدراسة الفعالية والمخاطر المرتبطة باستخدام الخلايا الجذعية الجنينية على المدى الطويل تم العثور على نتائج مماثلة في الحيوانات الصغيرة.
تصليح المفصل
يعد
الفصال العظمي السبب الرئيسي لآلام المفاصل في كل من الحيوانات والبشر. تصاب في معظم الأحيان الخيول والكلاب بمرض التهاب المفاصل. تجديد الغضروف الطبيعي محدود جدًا ولا يوجد أي علاجات أو
عقاقير شافية حاليًا، وإنما ننظر إلى تقليل الأعراض المصاحبة للتنكس. لا تزال أنواع مختلفة من الخلايا الجذعية المتعلقة باللحمة المتوسطة والمواد الأخرى المضافة قيد البحث للعثور على أفضل نوع من الخلايا وأفضل طريقة لعلاج طويل الأمد
إن خلايا اللحمة المتوسطة الدهنية المشتقة هي الأكثر استخدامًا حاليًا بسبب الحصاد غير الغزوي. وكان هناك الكثير من النجاح مؤخرًا في حقن الخلايا الجذعية المتعلقة باللحمة المتوسطة مباشرة في المفصل. هذه تقنية غير غزوية تم تطويرها مؤخرًا لتسهيل الاستخدام السريري. وأظهرت الكلاب التي تتلقى هذا العلاج مرونة أفضل في المفاصل وألم أقل.
إصلاح خلل العظام
إنه لمن الضروري وجود المزيد من الدراسات التي توصف تمامًا طريقة استخدام العلاجات المستندة إلى الخلايا لعلاج كسور العظام، لدى العظام عملية شفاء طبيعية فريدة وموثقة جيدًا، وهي في العادة كافية لإصلاح الكسور والإصابات الأخرى الشائعة. إن الفواصل المنحرفة نتيجة لصدمة شديدة، أو نتيجة لأمور مثل استئصال ورم من سرطان العظام، تكون عرضة لتضميد الجراح غير اللائق إذا تركت للعملية الطبيعية وحدها. يتم تصنيف السقالات التي تتألف من مكونات طبيعية واصطناعية مع الخلايا الجذعية الوسيطة ويتم وضعها في العيب. في غضون أربعة أسابيع من وضع السقالة، تبدأ العظام التي شكلت حديثًا بالتداخل مع العظام القديمة خلال 32 أسبوع، ويتحقق الاتحاد الكامل إن مزيدًا من الدراسات لازمة لتوصيف استخدام العلاجات المستندة إلى الخلايا لعلاج كسور العظام.
تم استخدام الخلايا الجذعية لعلاج أمراض العظام التنكسية أيضًا. إن العلاج الموصى به عادة للكلاب التي تعاني من مرض ليغ كالفيه بيرثيز هو إزالة رأس
عظم الفخذ بعد أن يقدم على الانحطاط. مؤخرًا، تم حقن الخلايا الجذعية الوسيطة مباشرة في رأس عظمة الفخذ، مع نجاح ليس فقط في تجديد العظام، ولكن أيضًا في الحد من الألم
الخلايا الجذعية وإصلاح العضلات
وقد استخدمت بنجاح الخلايا الجذعية لتحسين الشفاء في قلوب الكلاب بعد إصابتهم باحتشاء عضلة القلب. أزيلت الخلايا الجذعية المشتقة من الخلايا الدهنية ونخاع العظم وتم وضعها على خلية قلبية قبل حقنها في
القلب. بعد أربعة أسابيع من تطبيق العلاج بالخلايا الجذعية تبين أن انقباض القلب تحسن وأن هناك انخفاض في المنطقة المتضررة
هنالك تجربة مختلفة جارية حاليًا لرقعة مصنوعة من مادة مسامية يتم زراعة الخلايا الجذعية فيها من أجل تحفيز تجديد الأنسجة في عيوب القلب. تجددت الأنسجة واندمجت الرقعة بشكل جيد في أنسجة القلب. ويعتقد أن سبب ذلك يعود، في جزء منه، إلى تحسين الأوعية الدموية والحد من الالتهابات. وعلى الرغم من أن الخلايا الجذعية المتعلقة باللحمة المتوسطة أنتجت (cardiomyocytes)، إلا أنها لا تبدو منقبضة . العلاجات الأخرى التي يسببها مصير القلب في الخلايا قبل الزراعة حققت نجاح كبير في خلق أنسجة القلب المنقبضة
الخلايا الجذعية وإصلاح الجهاز العصبي
تعد إصابات
النخاع الشوكي واحدة من الصدمات الأكثر شيوعًا التي تجلب إلى المستشفيات البيطرية تحدث إصابات
العمود الفقري بطريقتين بعد الصدمة: الضرر الميكانيكي الأساسي، وفي العمليات الثانوية، كما في الالتهابات وتشكيل الندب، في الأيام التالية للصدمة. هذه الخلايا المشاركة في الاستجابة للأضرار الثانوية تفرز العوامل التي تعزز تشكيل ندبة وتمنع تجديد الخلايا. يتم تحميل الخلايا الجذعية الوسيطة المحثة على الخلايا العصبية إلى سقالة يسهل اختراقها، ومن ثم يتم زرعها في موقع الإصابة. تفرز هذه الخلايا والسقالة عوامل مضادة لتلك التي تفرز من قبل خلايا تشكيل الندب وتشجع على التجديد العصبي. وبعد ثمانية أسابيع، أظهرت الكلاب المعالجة بالخلايا الجذعية تحسن هائل على تلك المعالجة باستخدام العلاجات التقليدية. كانت الكلاب المعالجة بالخلايا الجذعية قادرة على دعم وزنها من حين لآخر، وهذا لم يظهر في الكلاب المعالجة باستخدام العلاجات التقليدية.
إن العلاجات موجودة أيضًا في
التجارب السريرية؛ لإصلاح وتجديد الأعصاب الطرفية. إن الأعصاب الطرفية أكثر عرضة للتلف، ولكن آثار الضرر ليست منتشرة كما رأينا في إصابات النخاع الشوكي. العلاج حاليًا في التجارب السريرية لإصلاح الأعصاب المقطوعة، مع النجاح المبكر. الخلايا الجذعية المستحثة لمصير عصبي تحقن في العصب المقطوع. في غضون أربعة أسابيع، لوحظ تجديد في الخلايا الجذعية التالفة سابقًا، وتشكل حزم عصبية جديدة تمامًا
والخلايا الجذعية هي أيضًا في المراحل السريرية للعلاج في
طب العيون. وقد استخدمت الخلايا الجذعية المكونة للدم لعلاج قرح القرنية من أصل مختلف من عدة خيول. وكانت هذه القرحة المقاومة للعلاجات التقليدية المتاحة، ولكن وردت بسرعة على نحو إيجابي في العلاج بالخلايا الجذعية. وكانت الخلايا الجذعية أيضًا قادرة على استعادة البصر في عين واحدة من حصان مع انفصال الشبكية، مما يسمح للحصان بالعودة إلى الأنشطة اليومية.
التهاب القرنية والملتحمة الجاف (KCS)
وقد توجت نماذج ما قبل السريرية لمتلازمة Sjögrens في اللجان الدائمة خيفي زرع حول الغدد الدمعية في الكلاب ش.م.ك التي كانت تخضع للعلاج الحالي. نرى تحسن كبير في عشرات في تصريف العين، فرط الدم الملتحمة، والتغيرات القرنية وشيرمر الاختبارات المسيل للدموع (اس تي تي)
المناطق الحالية للبحث
الخلايا الجذعية في المختبر
القدرة على نمو أنسجة بالغة وظيفية إلى أجل غير مسمى من خلال التمايز يخلق فرصًا جديدة للبحث المتعلق بالأدوية. الباحثون قادرون على تنمية خلايا متمايزة مختلفة ثم اختبار عقاقير جديدة على كل نوع من الخلايا لدراسة التفاعلات الممكنة في المختبر قبل تنفيذ الدراسات داخل جسم الإنسان. هذا أمر بالغ الأهمية في تطوير عقاقير لاستخدامها في البحوث البيطرية بسبب إمكانية حدوث تفاعلات محددة لكل صنف. الأمل هو أن وجود هذه الخلايا المتاحة للاستخدام في البحوث سوف يقلل من الحاجة إلى استخدام الحيوانات في التجارب؛ بسبب الآثار المترتبة على الأنسجة البشرية في المختبر ستوفر نظرة ثاقبة لا تعرف عادة قبل مرحلة التجارب على الحيوانات.
مع ظهور الخلايا الجذعية المحفزة (التوجيهية) أصبحت عملية تصنيع الأدوية وتركيبها أكثر اتساعا وأصبحت تستخدم لإنقاذ الحيوانات المعرضة لخطر الانقراض. بدلا من الحاجة إلى حصاد الأجنة أو البيض، والتي هي محدودة، يمكن للباحثين إزالة الخلايا الجذعية الوسيطة بسهولة أكبر والحد بشكل كبير من الخطر على الحيوانات بسبب تقنيات غير غزوية. وهذا يسمح للبيض المحدود أن يطرح للاستخدام لأغراض التناسل فقط.
الخلايا الجذعية وحفظها
ويجري استكشاف الخلايا الجذعية لاستخدامها في جهود الحفاظ. تم حصد خلايا بزرة النطفة الجذعية من جرذ ووضعها في مجموعة فئران، حيث أنتجت حيوانات منوية ناضجة تمامًا، وقادرة على إنتاج ذرية قابلة للحياة. البحث جارٍ حاليًا للعثور على خلايا مضيفة مناسبة لإدخال خلايا بزرة النطفة الجذعية المانحة. إذا كان من الممكن أن يصبح هذا خيارًا قابلًا للتطبيق، يمكن أن تنتج الحيوانات المنوية من الأفراد ذو النوعية الوراثية العالية الذين يموتون قبل الوصول إلى مرحلة النضج الجنسي، والحفاظ على هذه الخلايا التي ستضيع لولا ذلك.
الاستخدامات السريرية في المستقبل
يعد استخدام الخلايا الجذعية لعلاج
أمراض الكبد في كل من البشر والحيوانات محور اهتمام كبير. لدى
الكبد بعض الخصائص الطبيعية على التجدد، ولكن غالبًا ما تكون غير كافية للتعامل مع حدة بعض هذه الأمراض. وقد تم تشكيل
خلايا الكبد من بعض مصادر MSC، لكنها لم تطبق سريريًا بعد. وهناك جهد كبير لخلق خلايا جذعية متباينة على طول خط البنكرياس كعلاج محتمل لمرض السكري، ولكن لم يتم إنشاء هذا الخط جيدًا
الخلايا الجذعية الوسيطة هي حاليا قيد التجارب السريرية كعلاج محتمل لداء الطعم حيال الثوي ( مرض الرفض المناعي ) و رفض الطعم بعد عدة تجارب على الحيوانات المختلفة تبين فيها أن العلاج بالخلايا الجذعية الخيفية لم يرفض ولم يظهر أي اختلاف في قدرات الشفاء مقارنة مع الخلايا الجذعية ذاتية المنشأ. و يتم البحث في هذا المجال حاليا لاستخدام الخلايا الجذعية الخيفية في الطب البيطري التجديدي إن التجارب السريرية جارية لاستكشاف خصائص المناعة المنخفضة للخلايا الجذعية واستخدامها المحتمل لعلاج مشاكل المناعة المفرطة في الأشخاص الذين يعانون من الحساسية واضطرابات المناعة الذاتية
في السنوات الأخيرة، ظهرت عيادات الخلايا الجذعية في الولايات المتحدة لمعالجة المرضى باستخدام نخاع العظم الخاص بهم أو باستخدام الخلايا الجذعية الدهنية المشتقة البالغة كجزء من التجارب السريرية أو باستخدام برامج IRB المصرحة من إدارة الأغذية والعقاقير، وبالأخص للرياضيين ليتعافوا من الإصابات المتعلقة بال(osteoskeletal) (العظام، المفاصل
والنسيج الضام). ويناقش (Rudderham) ظهور العلاج باستخدام الخلايا الجذعية للبالغين في مقالته التي كتبها عام 2012 "العلاج باستخدام الخلايا الجذعية للبالغين في الولايات المتحدة"(Adult Stem Cell US Therapy).
تحتاج أن تدرس آثار هذه العلاجات طويلة الأمد خارج مساهمتها في الطب. إن التحسينات الواسعة في مجال الطب البيطري سمحت للحيوانات المرافقة ولحيوانات المزارع بعيش حياة أطول. هذا، ومع ذلك، فقد ساهم في ارتفاع الإصابات
والأمراض المزمنة في الحيوانات الأليفة العلاج بالخلايا الجذعية، وخاصة لعلاج قضايا جراحة تقويم العظام في الخيول، يسمح للحيوانات بالعودة إلى الحالة الطبيعية من النشاط في أسرع معدل مع انخفاض في معدل إعادة الإصابة.
الجدال حول الخلايا الجذعية الجنينية
المقال الرئيسي: الجدل حول الخلايا الجذعية
هنالك جدل كبير حول استخدام الخلايا الجذعية الجنينية البشرية. يستهدف هذا الجدل في المقام الأول التقنيات المستخدمة لاستخلاص خلايا جذعية جنينية جديدة، والتي غالبًا ما تتطلب تدمير
الكيسة الأريمية. وغالبًا ما يكون الاعتراض على استخدام الخلايا الجذعية الجنينية مبني على الاعتراضات الفلسفية أو الأخلاقية أو الدينية. وهنالك أبحاث أخرى عن الخلايا الجذعية التي لا تنطوي على تدمير الأجنة البشرية، وتتضمن مثل هذه الأبحاث الخلايا الجذعية لدى البالغين، الخلايا الجذعية السلوية والخلايا الجذعية المحفزة متعددة القدرات.
حول العالم
الصين
مارست جمهورية الصين الشعبية أبحاث عن الخلايا الجذعية والعلاج باستخدام الخلايا الجذعية. وسمحت وزارة الصحة في جمهورية الصين الشعبية باستخدام العلاج بالخلايا الجذعية لظروف خارجة عن تلك المعتمدة في الدول الغربية. وكانت الصين تحت رقابة الدول الغربية لفشل محاولاتها بتلبية المعايير الدولية لتوثيق هذه التجارب والاجراءات
تعالج الشركات التي تمولها الدولة الموجودة في منطقة شنزن هاي-تيك أعراض اضطرابات عديدة باستخدام خلايا البالغين الجذعية. وتركز شركات التطوير حاليًا على علاج
الاضطرابات العصبية والقلبية الوعائية. ويعد علاج
المخ باستخدام خلايا البالغين الجذعية من أكثر النجاحات الراديكالية التي قامت بها الصين. تقوم هذه العلاجات بإعطاء الخلايا الجذعية مباشرة في أدمغة المرضى الذين يعانون من
شلل دماغي، مرض الزهايمر، وإصابات الدماغ.
الشرق الأوسط
منذ عام 2008 حاول العديد من الأطباء والمراكز مجموعة من الأساليب المتنوعة؛ استخدمت في لبنان تقنيات تكاثرية وغير تكاثرية، في الجسم الحي وفي المختبر. وأخذ الطب التجديدي مجراه في الأردن ومصر
المكسيك
تمارس المكسيك حاليًا العلاج باستخدام الخلايا الجذعية على مستوى سريري. ويطلب تصريح وزارة الصحة الدولية(COFEPRIS). يوجد مراكز مرخصة في تيخوانا، غوادالاخارا وكانكون. و يخضع حاليًا لوس كابوس لعملية الموافقة. إن وجود هذا التصريح يسمح باستخدام الخلايا الجذعية.
كوريا الجنوبية
في عام 2005، أدعى علماء من كوريا الجنوبية أنهم استطاعوا أن ينتجوا خلايا جذعية مصممة لتتناسب مع المتلقي. وطورت كل من ال11 خلية جذعية جديدة باستخدام تكنولوجيا نقل نواة الخلية الجسدية (SCNT). واعتقدوا أن الخلايا الناتجة ستتناسب مع المادة الوراثية للمتلقي، مما يوحي أن نسبة رفض الخلية ستكون ضئيلة أو معدومة.
تايلند
اعتبارًا من عام 2013، لا تزال تايلند تعتبر أن زراعة الخلايا الجذعية المتعلقة بالدم هي تجريبية فقط. بدأ كامبون سريواتاناكول تجربة سريرية في أكتوبر 2013 باستخدام 20 مريض. سيتلقى 10 منهم العلاج لمرض السكري النوع 2 باستخدام الخلايا الجذعية وال10 الآخرين سوف يتلقوا العلاج
لانتفاخ الرئة باستخدام الخلايا الجذعية أيضًا. يقوم بحث كوتينانتاكول على الخلايا المكونة للدم ودورها في وظيفة الجملة المكونة للدم في التوازن والاستجابة المناعية
أوكرانيا
حاليًا، يسمح لأوكرانيا بإجراء تجارب سريرية للعلاج باستخدام الخلايا الجذعية (ترتيب الMH أوكرانيا رقم 630 "حول تنفيذ التجارب السريرية للخلايا الجذعية"، 2008) لعلاج هذه الأمراض: نخر البنكرياس،
تليف الكبد، التهاب الكبد، أمراض الحروق، مرض السكري،
التصلب المتعدد، نقص تروية الأطراف السفلية الحاد. أول مؤسسة طبية منحت الحق لإجراء تجارب سريرية أصبحت "معهد العلاج الخلوي" (كييف).
الدول الأخرى
بلدان أخرى حيث قام الأطباء ببحوث، وتجارب، وتلاعب، وتخزين، وعلاج الخلايا الجذعية: البرازيل، قبرص، ألمانيا، إيطاليا، فلسطين، اليابان، باكستان، الفلبين، روسيا، سويسرا، تركيا، المملكة المتحدة والهند وغيرها الكثير.

















 --------------
-------------- Solar System Ppt by AnnieFourman
Solar System Ppt by AnnieFourman  Solar System Facts Slideshow by K3TeacherResources
Solar System Facts Slideshow by K3TeacherResources  Best ppt on solar system by Make Megenius
Best ppt on solar system by Make Megenius The Solar System Presentation by 13lowect1
The Solar System Presentation by 13lowect1  Solar System by google
Solar System by google